|
拙著「企業の実験・大学の実験-反応工学実験の作法-」の補足資料として付けたものです。全体の目次は → こちら
https://onl.bz/YeZ3SC (アマゾン)
周知のとおり、ハーバー・ボッシュ法によるアンモニア合成技術は、二十世紀初期の画期的業績である。現在では文献も多く、ハーバーやボッシュの伝記的な記述だけでなく、開発経緯・結果についての科学技術史的、理工学的な観点からの言及も少なくない。現在も基本的には殆ど変わらず用いられている代表的な化学プロセスであるから、ネットから情報を得ることも容易である。
このアンモニア合成法の開発には、化学平衡、反応速度、触媒化学、気液平衡、物質・熱収支、また、高温の材料科学、硫黄、塩素などの微量阻害成分の処理、ガス圧縮装置を含めた全体プロセスの最適設計など、反応工学の主要な課題の殆どが含まれている。先の本篇の具体例として記述するには荷が重いが、また原典に当たるなどの精細な探索調査によるものでもないが、先人の労苦に思いをはせるとともに、理論との整合性、チームワーク・実験現場の重要性、実験の失敗と思わぬ幸運、安全対策、特許権の争いなど、本篇にのべた事項を念頭に関連書籍や報告をもとにまとめ、併せて、現在の地球温暖化などのエネルギー・環境問題に関する内容を適宜加えたものである。
科学史は専門ではないので、正確を期したつもりではあるが、歴史的事実などの記述に誤りがあるやも知れず、読者諸氏のご叱正、ご教示を頂ければ幸いである。
コールタール利用の染料工業
それまでの錬金術を脱し、ボイルを経て、ラボアジェらによって近代化学の基礎が築かれたのは十八世紀後半から十九世紀初めにかけてであり、徴税人でもあったラボアジェが「共和国に化学者はいらない」としてフランス革命の断頭台の露と消えたのは1794年のことである。化学工業としては、まず無機化学をもとにしたソーダ工業、硫酸工業が、英国産業革命の端緒となった紡績産業を牽引することになった。1791年のルブラン法炭酸ソーダの発明などが、その顕著な成果である。十九世紀半ばには、有機化学を基礎とする染料工業が、まず英国でおこり、ついでドイツでおおいに発展することとなった。これは、それまで貴重で高価であった
藍
や
茜
などの天然物である染料を、人工的に化学合成しそれに代替するものである。図1に、二十世紀中期の石炭化学工業の概略系統図を示したが、コールタール利用の原点は、染料工業にある。

図1 二十世紀中期の石炭化学工業の概略系統
英国人ウイリアム・マードックが石炭ガスを用いて、初めてガス灯をともしたのは1792年のことであるが、1867年、瓦解直前の江戸幕府外国奉行であった栗本
鋤
雲
は、フランスパリを視察して、「気灯の源は
巴里
の外にあり。大鉄炉を設け、
石楳
を焼き、鉄管を以て地下に通じ、枝管
旁
布
し至らざる処なく、以て其
気
を通じ毎灯
引
て以て点明す。(中略)。気灯の街上を照す、其
明
、俯して虫蟻を拾ふべし。故に暗黒夢月の夜、風雨
晦冥
の際と雖も、その行歩を
礙
げず。又其気極めて
煖
かなれば、人家引て暖炉に換ゆるものあり」と書いているc)。気灯はガス灯、石楳は石炭のことであり、パリやロンドンなどの大都市では石炭ガスが、照明や暖房に一般にも広く利用される時代となっていたのである。わが国では、この紀聞より五年後の1872年(明治5年) 、横浜に十数基が灯されて維新文明開化の一つの象徴となったことは周知の通りである。
石炭を、空気を断って1000℃程度で乾留すると、製鉄用のコークス、上述の照明用などの燃料となる石炭ガスとともに、液状のコールタールが得られる。コールタールは十九世紀中頃まで、用途のない厄介な廃棄物であり、ドイツのリービッヒはその有効利用に大きな興味を持っていた。その弟子であるホフマンは、アニリン(アラビア語で青の意味から命名された)の研究で著名であったが、若くして英国に招かれ、そこで20年間多くの英才を指導することになった。そのうちの一人がパーキンであり、まだ一八歳の時、マラリアの特効薬であるキニーネを、タールから得るための化学合成実験中に、思いがけず美しい赤紫色の染料を見出すという幸運に恵まれた。自分の粗末な実験室で、復活祭の休暇中のこととされる。染料はそれまではすべて動植物から得られていた。ある種の昆虫からの
臙脂
色、アッキ貝からの古代紫、サフランからの
橙
色、
茜
からの暗赤色など、古来より貴重であったそれらの発見や製造の歴史は、神話や伝説などを含め様々な興味深い物語で彩られている。それが今、18歳の若者によってはじめて実験室で化学的に合成されたのである。
パーキンは、色が似ている花の名からそれをモーブと名付けた。石炭から、美しい染料が得られたことは世の注目をひき、その後大量にでてくる合成染料の嚆矢となったものである。後述のアンモニア直接合成の時には「石炭と空気からパンを作る」といわれ、さらにその約30年後のウォーレス・カロザースのナイロン合成(1935年)に際しては「石炭と水と空気から作られ、鋼鉄よりも強く、クモの糸より細い」といわれたが、石炭という有機質高分子は一般の人にとっては黒い塊にすぎず、このような標語に強いアピール効果があったのであろう。ちなみに、ナイロンはそれまで生糸、絹織物が輸出の大部分を占めていた当時の日本にとって大打撃となったが、これに発奮した研究者、技術者による合成繊維ビニロンの発明、国産化に繋がったのは周知の通りである。
ホフマンが英国からドイツに戻ってからは、ドイツが合成染料工業の中心となる。植民地からの天然物が入手できる英国は、それほど力を入れなかったこともあるが、やはり研究指導者の存在は大きい。人工の茜染料であるアリザリン(下図左)は、ドイツBASF社(Badische Anilin - u. Soda ?Fabrikの略であるが、1973年以降は略称の
BASF
が正式な社名になっている)のカール・グレーベらによってアントラセンを基本に合成され、1869年6月25日に特許出願された。上述のパーキンも同時期に合成に成功したが、特許出願は惜しくも数日遅れであった。このこともあって、その後の染料工業におけるドイツの優位は動かぬものとなった。アリザリンは化学合成による天然染料代替の最初の本格的商業化例となった。
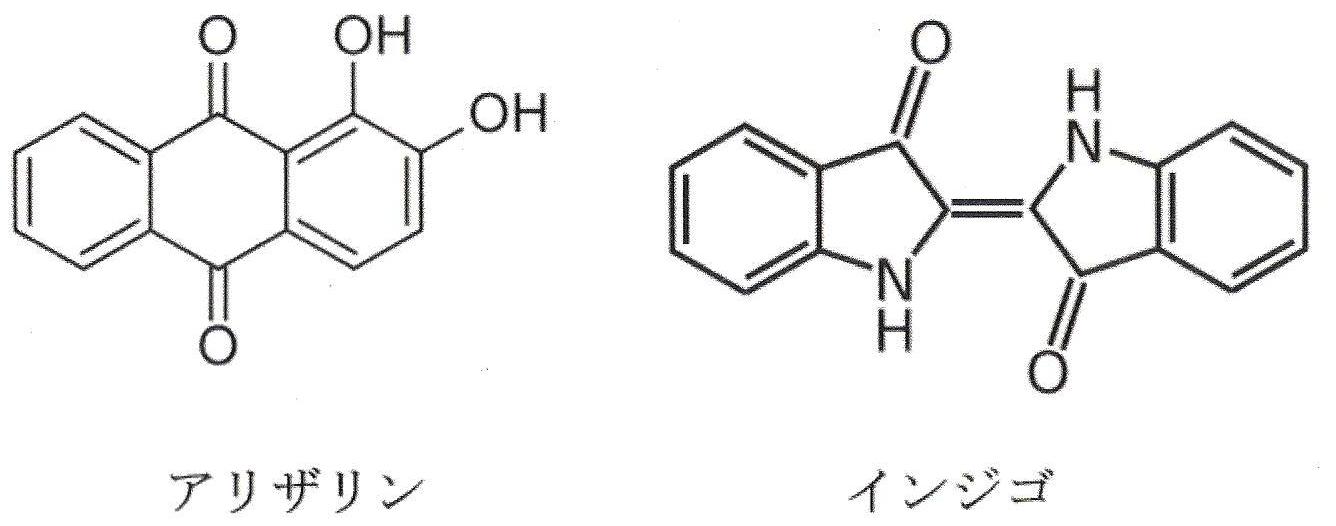
次に古来珍重されていた藍の合成である。天然藍は当時、特産地であるインドから欧州各地へ輸出されていた。その化学構造はドイツのバイヤーによって、20年近い苦心のすえ決定された(上図右)。バイヤーがはじめてインジゴを人工的に合成したのは1878年である。ただ、初期の合成プロセスでは、コスト的にはまだ天然藍に及ばず、多くの企業がその工業化にしのぎを削ることになる。ここで先にアリザリンを商業化し、本主題のアンモニア直接合成法開発の主役となるBASF社が再び登場する。責任者は技術部長の立場にあり、のちに会長となるハイリンヒ・フォン・ブルンクであった。ベンゼンの六員環構造の提唱で著名な、かのケクレ教授の弟子である。BASF社がインジゴの工業化に成功したのは一八九七年であり、十年余の苦闘の間に育まれた技術力が、そのあとのアンモニア合成をはじめとする高圧化学工業展開のための基盤となる。1865年の創業時には一介の染料会社にすぎなかったBASF 社であるが、ブルンクの確固たる方針のもと、染料やそのほかの化学製品開発のために、1899年時点で既に150人の化学者を集めていた。150年以上の歴史を持つBASF社は、現在世界最大の総合化学会社である。
ちなみに、日本で最初の合成染料製造に成功したのは、下村孝太郎と三好久太郎であった。下村は1914年8月14日の夜、10年前の自らの実験ノートをもとに京都の自宅でナフタレンの硝化反応の実験中、爆発により両眼の視力を殆ど失った。三好がそのあとを継ぎ、ナフタレン原料の新規染料合成に成功したが、下村の探求心はその後も衰えず、懇請されて染料会社の技師長を引き受け、この国策会社の技術面を取り仕切った。子息へ与えた遺訓の一つに「技術者は機械にあらず、機械を支配する職なれば、人生を弁じ、人間を支配する能力なかるべからず」とある。
直接アンモニア合成法開発の前夜
前にもあげたドイツのリービッヒが、「植物の栄養は、土壌から吸収する無機元素である」と主張したのは十九世紀の中葉、1840年のことである。ただ、植物栄養学の祖といわれるリービッヒも「窒素は空中からアンモニアの形で供給されるので、肥料としては不要である」との誤った見解を示している。窒素を含む植物必須10元素説が確立されたのは、それから20年後である(現在では17元素にまで増えている)。
既にマルサスはその「人口論」(初版1798年)で「人口は幾何級数的に増えるが、食料などの生活物資は算術級数的にしか増加しない。したがって貧困は永久になくならない」として、救貧制度の弊害を主張し、早婚の禁止を説いていた。1850年代の欧州は、産業革命の進行によって人口が急速に増大し、農産物をはじめ食料不足が深刻になりつつあった。リービッヒに触発された研究によって、肥料の三要素として、窒素、リン、カリの効果が知られており、このうちリン、カリについては対処可能の見込みができつつあったが、窒素が難題であった。
まずは窒素とリン酸塩を多く含むペルーからのグアノ(海鳥糞)が用いられた。アミノ酸の分解で生じるアンモニアは動物にとって有害であり、早急に体外へ放出する必要がある。魚類などは水中に溶解できるからアンモニアのまま、我々哺乳類などは、毒性のない水溶性の尿素の形で排出するが、鳥類は毒性が低く水には溶けにくい尿酸に替えて排泄する。糞中にある白いものが尿酸である。このグアノが枯渇してくると、チリ硝石に頼ることになったが、それも急速な人口増にいつまで対応できるか、心もとない状況で、欧州全体が危機感にとらわれていたのである。チリ硝石は火薬のもとでもあった。火薬は古くから可燃物である木炭、硫黄に酸化剤である硝石(硝酸カリウム)を混合して作られた。黒色火薬と呼ばれるが、チリ硝石に含まれる硝酸ナトリウムでは爆発性が弱く、硝酸カリウムに変えて用いられていた。1867年、アルフレッド・ノーベルによってダイナマイトが発明され、黒色火薬にとってかわると、チリ硝石は今度はニトログリセリン製造のための硝酸の原料として用いられることになった。
このような状況を受けて、著名な物理学者であり、タリウムの発見者でもある英国のクルックス卿は、1898年(明治31年)、英国科学アカデミー協会の会長就任にあたって70分にもわたる演説を行い、「英国をはじめすべての文明国家は今、来たるべき人口増と食糧難で生死の危機に瀕している。この暗黒の中にも一条の光はある。それは空気中の窒素の固定であり、窒素から導かれるアンモニアは肥料のもとになり、また硝酸は火薬の原料になる。これこそ化学者の才能に待つべき偉大な発明の一つである」として、特に化学者を指定して鼓舞した。
その成果はすぐにあらわれ、空中窒素の固定法として、1903年にノルウェイで高電圧電弧法、1906年には石灰窒素法がドイツ、イタリーで工業化された。
高電圧電弧法は、アーク放電の高温度で空気中の酸素と窒素を化合させるもので、今でいう燃焼時火炎後流での窒素酸化物(NOX)生成、即ち(1)式で示されるサーマルNOXの生成反応そのものである。しかしエネルギー効率は三%といわれるから、電力コストを考えればノルウェイのような水力発電に適した所でなければ困難である。
N2 + O2 → 2NO (1)
硝酸は、このNOを低温度で空気または酸素で酸化してNO2とし、水に吸収させてつくられる。本篇出紹介した宇田川榕菴「舎密開宗」で記した方法、「消酸(硝酸)ハ窒素酸素ヲ以テ成ル者ナリ、窒素瓦斯ニ酸素瓦斯ヲ和シテ越列機火ヲ通スレバ、消酸ヲ生シ・・・」そのものである。肥料としては、硝酸と石灰を反応させ、硝酸カルシウムの形で用いられた。なお硝酸は、現在では殆どが、後述のアンモニアを原料とするオストワルド法でつくられる。
一方、石灰窒素法でのアンモニア製造法は、反応式で示せば、
CaO+3C → CaC2+CO (2)
CaC2+N2 → CaCN2+ C (3)
CaC2+3H2O → NH3+CaCO3 (4)
となる。これが、世界初のアンモニアの工業的製造法であり、現在もまだ一部で使われているが、(2)式のカーバイド(CaC2)の生成に大量の電力を使い、製造原価が高い難点がある。
最も期待されたのは、やはり水素と空気中の窒素とを直接化合させて、アンモニアを合成する方法である。
アンモニア直接合成法
アンモニアの直接合成は反応式で示せば、
N2+3H2 → 2NH3 +91.88kJ/mol ( 発熱) (5)
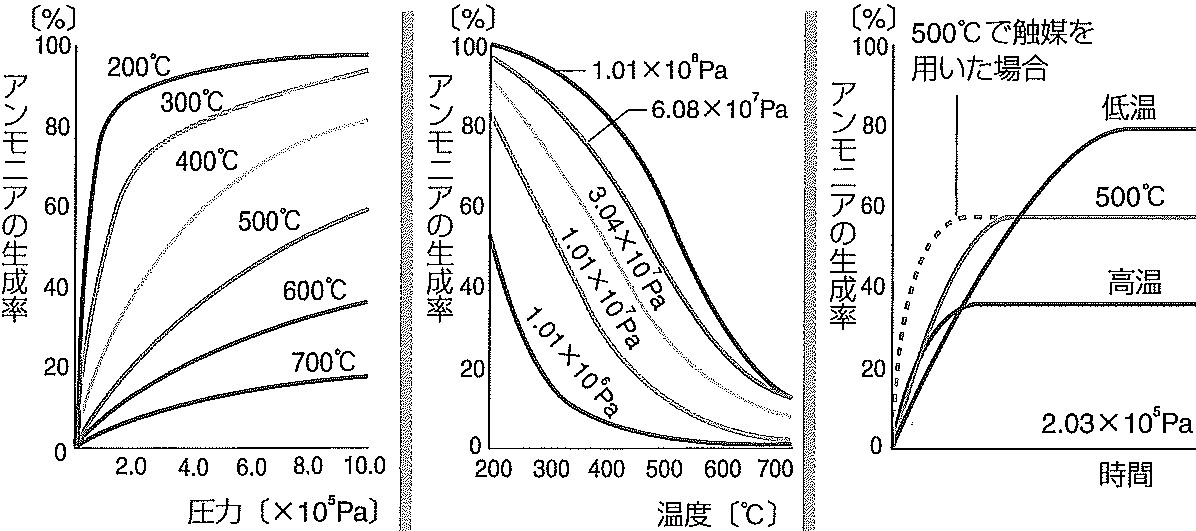
図2 アンモニアの生成率に及ぼす圧力、温度、触媒の影響
|
となる。従って、ル・シャトリエの法則によって、アンモニアを効率よく得るには、低温高圧ほど望ましく、また低温で反応速度が実用的でなければ、適切な触媒を用いれば良い、というのは高校化学の知識である(図2)。また関連するN2、H2 、NH3の三分子について、それぞれの標準生成エンタルピー、標準エントロピー、および温度の関数とした比熱のデータを与え、この反応の化学平衡について、温度と圧力依存性を定量的に計算させるのは、化学専攻学生の「物理化学」の演習問題である。
もとより現在の知識によればであって、当時はこのような熱力学を含む物理化学の揺籃、発展期であり、ドイツのヴィルヘルム・オストワルドと、ヴァルター・ネルンストはその主導者であった。
クルックス卿の刺激的な所信表明から二年後の一九〇〇年、ベルリン大学の物理化学教授オストワルドは、水素と窒素からアンモニアを生成することに成功したと主張し、BASF社に工業化の話を持ち掛けた。触媒の先駆的な研究者である彼は、加圧のために自転車用空気ポンプを使ってさまざまな材料を試し、有望な触媒を見出したという。それに対応したのが、BASF社に入社間もない二六歳の技術者カール・ボッシュであった。ボッシュは中央研究所で、ナフタレンの硫酸酸化によるフタル酸製造部署に所属していた。その部長は、偶然の僥倖からフタル酸製造反応での水銀の触媒効果を発見したオイゲン・サッパーであった。温度計が壊れて、それから流れ出した水銀が有効に作用したのである。ボッシュは当初より触媒には縁が深かったとみえる。
ボッシュは急遽、実験装置を組み立て、オストワルドのいう鉄のらせん(針金)を触媒として、試験を行ったが、なぜかアンモニアは生成しなかった。その報告を聞いたオストワルドは議論のためBASF社にやってきた。若く未経験なボッシュの実験に誤りがあるのではと疑ったのである。ボッシュも、高名な教授が誤る筈はないと思いながら、今度はオストワルドから提供された鉄のらせんを用いて再実験を行った。しかし実験のはじめにはアンモニアが得られるものの、何回か繰返すうちにアンモニアは検出できなくなった。この結果に困惑したボッシュは図書館にこもって、アンモニアや鉄に関連する学術発表に目を通し、それらをもとに考察を加えた。そしてオストワルドの研究室では、合成試験の前に一度アンモニアを通したため、らせんの鉄が高温度で窒化し、それに反応ガスである水素が反応してアンモニアを生成したものに過ぎないと結論した。微少量の窒素の挙動に起因する誤認であり、反応器出入口の窒素分の収支からは判りようがないことではある。
オストワルドは、その報告を受けて再びBASFに乗り込んできたが、ボッシュとの白熱の議論の末、結局ボッシュの見解を認め、既に出願していた特許を取り下げた。オストワルドの研究室では、アンモニアの分解試験に、合成試験と同じらせん状の鉄を用いていたらしい。ボッシュは毅然として、この大学者の見落とし、実験ミスを指摘したのである。社内のボッシュに対する評価はこれでさらに高まった。
オストワルド法による硝酸製造
ここでは面目を失したオストワルドであったが、1902年には、白金を触媒にしたアンモニアの酸化によって硝酸を得る方法を提示している。オストワルド法と呼ばれ、現在も硝酸の工業的製造は、ハーバー・ボッシュ法で得られたアンモニアを原料として、この方法によっている。即ち、空気または酸素によってアンモニアからNOを得、さらにNO2として、これを水に吸収して硝酸とするもので、高校の教科書にもでている。従って、廉価なアンモニアさえできれば、火薬の原料である硝酸の供給に対する不安も消失することになる。
硝酸の工業用プラントの基礎は、後年、BASF社のボッシュ、ミタッシュらによりつくられた。オストワルドが用いた触媒は白金箔、BASF社の工業化(一九一四年)当時は鉄‐ビスマスであったが、現在では白金線(白金網)が用いられている。アンモニアからのNO生成部分の主要な反応を総括反応式で示せば、
4NH3+5O2 → 4NO+6H2O (6)NO生成主反応
4NH3+3O2 → 2N2+6H2O (7)望ましくない副反応の例
即ち、NOだけでなく窒素に転換されて無効になる分がある。これらはNH3と酸素の反応であるが、一旦生成したNOがNH3と反応して消費される下記反応は、この製法の研究に関連して1920年代に発見されたといわれる。
6NO+4NH3→ 5N2+6H2O (8)
その後、これに酸素が共存すると、次のように変化することも判った。
4NH3+4NO+ O2 → 4N2+6H2O (9)
現在、発電プラントなどからの排ガス中NOxの処理には、多くNH3を還元剤とする選択的触媒還元法が用いられているが、(9)式はその反応式そのものである。
さらに近年地球温暖化が問題になってからは、硝酸プラントからの副生成物として、少量ではあるが、亜酸化窒素(N2O)の生成が問題視され、触媒を用いたその分解装置での低減がはかられている(還元剤を要せず、N2Oは窒素と酸素に分解される)。周知のとおり赤外吸収能をもつN2OはNO,NO2とは異なり反応性が低いため大気中に百年以上滞留し、CO2の300倍の高い温室効果をもつ。BASF社は、最初の工業化より80年余の1998年、本法で生成するN2Oの分解触媒について特許出願しているb)。
以上に鑑みるに、硝酸製造装置の実用化当初は、反応機構や窒素分の物質収支の細部まで充分に把握されていたか、やや疑問ではある。検討はなされても、実用上特に問題なく、公表されなかっただけかも知れない。今となっては、こういう部分の事情に触れた資料に接することは容易ではないようである。
余談ながら、石炭、石油、或いはバイオマス中には窒素が含まれる。Fuel N(燃料中窒素)と呼ばれるが、この窒素は発電目的などの燃焼過程では、途中HCN(シアン化水素)或いはNH3の形を経て、最終的にはNOx或いはN2となる。勿論この場合、硝酸製造の場合とは逆に、無害なN2に転換される割合が高い方が好ましい訳である。また脱炭素がいわれる昨今、水素輸送の媒体の一つとしてNH3が検討されている。この場合も最終的な熱利用の段階でNOx抑制に留意して燃やせば、大半はN2に転換することができる。ただそれでも数百或いは数十ppmのNOxの排出があれば、脱硝装置での後処理が必要となろう。
思えば、NOxやNH3など、窒素、酸素、水素というありふれた元素から成る単純な分子の「化学」も連綿と続き、また今後も続いていくのである。
ハーバーの実験
話をもとに戻すと、化学を志しながら、職を求めて企業や大学を転々としたのち、フリッツ・ハーバーがカールスルーエ工科大学の物理化学、電気化学の教授の地位に就いたのは1906年、37才の時であった。ハーバーはその前年、鉄触媒を用いてアンモニア直接合成反応?式の平衡値を測定し、一気圧、1020℃で、アンモニア濃度0.012%の結果を得ていた。即ち常圧での試験である。一九〇七年五月ブンゼン協会の会合で、ハーバーは、絶対エントロピーの提唱者ネルンストとその結果について議論することとなった。ネルンストは、その値が自らの計算した理論値と比較して高すぎること、また自らの高圧(30‐75気圧)での測定結果からの推算とも整合しないことを示した。ハーバーは再試験を行い、ネルンストの見解の正しさをみとめた。
1908年3月6日、ハーバーはBASF社と、アンモニア合成ほかの研究に関する、最初の契約を結んだ。ハーバーが、その後のアンモニア合成試験で得た成果をもとに提案した研究内容に、BASF社が興味を示したのである。研究で得られた特許はBASF社に帰属し、許可なく成果の発表をしない条件となっていた。
核となるアンモニア合成反応部の条件設定の要点は、触媒存在下での化学平衡と反応速度のバランスである。ハーバーはBASF社の援助で装置を購入し、ネルンストの勧めもあり、高圧での触媒探索、反応温度、圧力などの条件選定、高圧下での生成アンモニアの分離、未反応ガスの循環法などの実験を継続した。圧力は100気圧から200気圧であった。当時、ハーバーの研究室にいて、ハーバーの四つの論文に名前のある田丸節郎が、アンモニアの生成熱と反応ガスの比熱を測定し、平衡定数の算出に貢献したことが知られている。
開発の鍵である触媒については、白金、ニッケル、マグネシウムなど多数について試したが、最も効果が認められたのは、たまたま実験室に残っていた電球用フィラメントのための材料、オスミウムであった。ハーバーは当時いろいろな研究に手を付け、また企業の顧問も引受けていたのである。もしこのオスミウムの残留物がなかったら、アンモニア合成の歴史は少しは変わったかも知れない。
1909年3月はじめ、BASF社の会長となっていたブルンクは、ボッシュを伴ってハーバーの実験室を見学した。まだほんの数滴の液体アンモニアができたに過ぎない段階であったが、インジゴの工業化での自信もあったのだろう、そこでこのハーバー方式の工業化を決断した。その時、ブルンク会長は操作圧力が100気圧と聞き、BASF社の工場では七気圧での圧力釜でも爆発したことで危惧したが、意見を求められたボッシュが自信を示したことで決断したとされている。ボッシュは溶鉱炉で働いた経験があり、機械工学を二年学んだあと、化学に転じたという経歴をもち、最新の鉄鋼業界の状況にも通じていた。
その4か月ほどのちの1909年7月のはじめ、ボッシュ、ミタッシュが、ハーバー研究室での連続運転に立ち会った。こういう改まった試験の場合に良くあるように、ガス漏れなどのトラブルがあったが、最後には、5、6時間の連続運転ができた。窒素のアンモニアへの転換率は6~7%、2時間でアンモニアは小さなフラスコいっぱいになった。
1910年3月18日、ハーバーはカールスルーエの自然科学協会の会合で、小型の実験装置を用い、アンモニア合成の公開実験を行った。量論比である1:3の窒素と水素ガスを一八五気圧で供給し、毎時80gのアンモニアを合成するもので、反応器高さは85cmであった(図3)。ネルンストは、ハーバーの成功を賞賛するとともに、自らの早すぎた撤退を悔んだといわれている。ただ、オストワルド、ネルンストの初期の実験、理論的貢献と助言もまた銘記されるべきは勿論である。
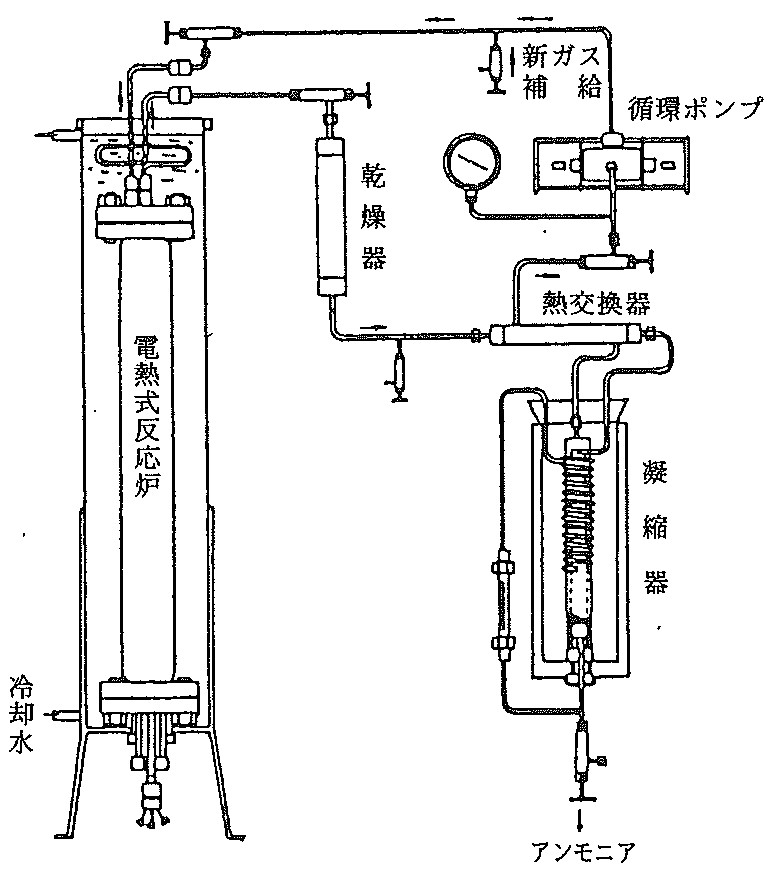
なおハーバーの最初の特許は、母国ドイツでは、1908年10月12日に出願された。日本では「アンモニア製造法」の名称で1909年(明治42年)10月4日に出願(工業所有権に関するパリ条約の優先権主張の期限12か月内ということであろう)され、翌1910年3月25日に特許17834号として登録されている。発明者はハーバーと、その協力者であったロッシニヨール、特許権者は前述契約の通り、BASF社である。その明細書は日本の特許庁のネット検索で見ることができるが、詳細な実験の方法、評価装置の構成、定量的な結果など、現在でいういわゆる「実施例」の記述はない。
ボッシュ、BASF社の開発
しかし、大学の実験室でのコア部分の成功と、経済的に採算がとれるプラントとしての工業化の成功は全く別である。当時は小容量密閉容器での加熱などの僅かな例外を除けば、殆どの工業的な化学操作は常圧で行われていた。ハーバーの実験は、実験者自身、またそれに立ち会った人々が等しく感動しても、実験台上の小さな反応装置、高圧に耐えるよう厚い石英の中を削りそれを金属で覆った反応器、稀少なオスミウム触媒であり、得られるのは少量のアンモニアであった。これを一日数トン、数十トンの規模とするためには、全体のプロセスを具体的に決定し、長期の安定運転が可能なものとしなければならない。反応器はもとより、高圧高温仕様の圧縮器、バルブ、配管、制御装置を含め補器類、最終的には何万点かに及ぶであろう部品の調達、或いは自製が必要である。
早速BASF社での開発が始まった。工業化のために差し当っての主要な課題は三つあった。実用的な触媒の選定であり、反応器の材質・構造の決定であり、最後に原料である水素の供給手段の策定である。
触媒については、ハーバーのオスミウムは高価で希少で、実用的なものを探索する必要があった。担当はオストワルドに学んだアルヴィン・ミタッシュであった。ミタッシュは昼夜連続運転が可能な小型高圧反応器30台を用い、2500種類の触媒について、100気圧、550℃での試験を6500回繰り返して、最終的に反応活性、寿命の点から磁性酸化鉄(Fe3O4)をベースにアルミナ、酸化カリウムを促進剤として加えたものを選定した。試験のための充填触媒量は2gで、カートリッジで交換可能となっていた。
ミタッシュの実験室は大きな地下室にあった。触媒は、最初は鉄に着目していたが、膨大な探索試験をへて、結局また鉄に戻った。思いがけず訪れた転換点は、スウェーデンから入手した磁鉄鉱でオスミウム並みのアンモニアが得られた時であった。他の磁鉄鉱では触媒効果が得られないこともあった。ミタッシュは、最新の報文を読んで、これは磁鉄鉱に含まれる不純物の効果ではないかと推量した。そして化学的に純粋な磁性酸化鉄にいろいろな物質を加えて系統的な試験を行った。この試験の最初期に試みたのが、結局最良の効果を示す、磁性酸化鉄、アルミナ、酸化カリウムの組み合わせであった。
現在の知識でいえば、実際に反応に寄与しているのは、還元された単体金属鉄、アルミナはその凝集防止の担体、カリウムは鉄への電子供与のための促進剤ということになる。オストワルドが用い、ハーバーが何百回も試した純粋な鉄ではうまくいかず、有効な作用をもつ不純物がある場合のみ効果が得られたわけである。また併せて硫黄などの触媒毒についての知見も得て、硫黄を含む鉄鉱石では触媒活性がなかったことも説明できた。ミタッシュはさらに実験をかさね、最終的には一〇年余で合計二万回に及ぶ実験を行ったとされる。
このミタッシュの、具体的で印象深い触媒探索のエピソードは、多くの関連資料に出てくる。当時は実験を数多くこなす以外になかったのであろう。触媒についての最初の系統的研究者はオストワルドであるが、それからさほどの時間も経過していないから、他に利用できるデータは殆どなかったであろうし、勿論、現在のような精緻な固体表面分析装置や触媒設計法などある筈もない。ミタッシュをはじめとする実験担当者の、最終的に一つの触媒を選ぶための日夜を分かたぬ多大な労苦があったことは容易に想像される。
次に、反応器の材質については、500~600℃、数百気圧という過酷な条件であり、当初からの大きな懸念対象であった。ボッシュは冶金の素養・経験があり、自らこの開発に当たった。アンモニア合成という典型的な化学プロセス開発の現場のリーダーがボッシュであったことは、特に材料の問題が深刻であったこともあり、一つの大きな幸運であったように思われる。問題は、高圧の水素が鋼材中の炭素をメタンにして引きぬくことによって脆くなる、いわゆる水素脆化である。ボッシュらは試行錯誤を重ねて、炭素含有量の少ない軟鋼を内張にした二重構造とするアイデアで解決した。それまでは、事故のため運転が二日以上続くことはなかった。反応塔の実験は工場跡で、一つ一つの反応塔を特別の鉄筋コンクリートのカプセルで覆って行われていたが、爆発が予想される状況になると、装置を解体・廃棄する以外になかったのである。それでも製造したアンモニアは高価で売却できて採算がとれたから、当時いかにアンモニアが貴重であったかが判る。このボッシュのアイデアが実装されて以降1か月の運転が可能となった。
最後の課題は水素の供給である。既に石灰窒素法でのアンモニア合成法が商用化されているから、それ以下の製品コストでなければ意味がない。工場設備費は巨額であるが、それを除けば製品コストに最も影響するのは、原料である高純度の水素である。現在では、アンモニア合成用の水素は殆どが天然ガスの水蒸気改質によって得られるが、当時は、水の電解または石炭のガス化改質による方法が候補であった。水力に恵まれないドイツでは電力は高価であるが、石炭(褐炭)は豊富であったから、結局、コークスを空気でガス化し、それに新規の鉄クロム系のCO転化装置などを組み込むことによって、経済的な水素製造が可能となった。なおアンモニア合成に必要なエネルギーの大半は、現在でも、原料である天然ガスなど化石燃料の熱量分を含めた水素製造に係る部分である。
アンモニア合成技術の工業化
大手染料化学会社ヘキストとの特許紛争も、1912年3月ハーバー、BASF社側の勝利で解決した。アンモニア製造装置は1911年には日産100?であったが、翌年には1トンとなり、1913年には一系列10トンの三系列、日産30トンの工場をドイツ南西部のオッパウに建設するに至った。毎年10倍のスケールアップだったことになる。その後も、装置の増強を続け製造能力は急速に伸びて、地球の裏側から硝石を船で運ぶ必要もなくなった。窒素供給の歴史的役割をはたしたグアノ(海鳥糞)は取り尽くされてしまったが、こうしてペルーとの戦争の末チリが勝ち取った硝石は、今もなお豊富に存在する。廉価なハーバー・ボッシュ法によるアンモニア直接合成に駆逐され、採掘の意義が失われたためである。ただ、その後の急激な人口増で、現在、世界のアンモニア生産に必要な窒素分をチリ硝石で賄おうとしても、それはわずか数か月可能なだけではある。
第一次世界大戦でドイツは敗れた。英国、フランスのように植民地を持たないドイツは、タイヤのための天然ゴムを得られず、しかもその石炭からの合成に(これにもBASF社が関与している)手間取ってしまった。結局、アンモニア合成の成功で爆薬の供給はできたが、砲車や兵士の移動で負けたとさえ言われた。
アンモニアの合成法は現在も基本的には殆ど変わらない工程であり、これらを殆どゼロの状態から短期間に工業化の段階にまで発展させたボッシュをはじめとする優秀な技術陣の奮闘とチームワーク、また経営責任者であるブルンクの決断、スピード感ある運営は高く評価されている。今日からすると意外なことに思えるが、1913年、これは日産30トンのプラントをオッパウに建設した年であるが、この段階に至っても、ある書では、巨大量、可燃かつ200気圧以上の水素ガスの危険性に鑑み、この成功の可能性を極めて低くしかみていなかったということである。即ち「もし何かの機会があれば、例外的に使用される事はありましょう。動かしているそのガス量は、いずれにしてもそれほど巨大なので、特別の場合以外には技術的・経済的な利用性並びに国民経済的な意味は殆ど考えられません」a)。
低炭素、脱炭素がいわれる現在、アンモニアを水素のキャリアとするため、より低い圧力、温度での合成法の研究開発が行われているが、それには高活性の触媒開発が必須となる。ただ、低圧になればガス体積が増大し機器や配管などプラントのサイズが大きくなり、また生成アンモニアの凝縮液化過程も厳しくなるから、用途までを含んだシステム全体としての評価が必要である。
ハーバー・ボッシュ法についての学術的解説や科学技術史的な論説は大変多いが、実験時の人身災害についての記述は、殆ど見当たらない。勿論当時のことであるから、少々の怪我や火傷の類はかなりの頻度であったであろうし、今となってはそのような詮索に余り意義もない。ただ、高圧高温、しかも可燃性、爆発性の水素を使うという、危険性が明らかなものであるから、万全を期していたことは、関連書籍の具体的記述からも充分に窺える。ボッシュ自身も、監督に当っていたある時、作業者が不注意から、装置を間違った管につけて大惨事を引き起こしそうになった際には、常になく激しく怒って、直ちにその当人を転任させたというから、安全については当然ながら意識が高かったに相違ない。ただ、製造工場での事故は免れなかった。1921年9月21日のオッパウ工場大爆発である。それもアンモニア合成プラントではなく、製品の貯蔵サイロであった。4500トンの硫安硝安の混成肥料が爆発し、従業員など500人以上が死亡した。それまで数年間、およそ三万回は無事故で済んでいた、一部の吸湿固化した肥料を出荷のため爆薬で崩す作業が原因であった。ボッシュは経営者として、また技術者として強い衝撃を受け、追悼式で痛苦に満ちた挨拶をしたあと、数か月は業務に戻ることができなかった。
メタノール合成、石炭液化などの波及技術
この多大な困難を克服してつくられた画期的なアンモニア合成技術をもとに、尿素合成、メタノール合成、石炭の液化などの高圧化学工業がBASF社を中心にして次々に工業化されていく。いずれも高圧でかつプロセスを直列的につなぎ原料から製品を得るという、それまでになかった新しい手法であり、これはその後の石油化学工業にも引き継がれていくことになる。
例えば、石炭を原料にしたメタノール合成は、簡略化して示せば、次のような化学反応である。
C+H2O → CO+H2 (10) (水性ガス反応)
CO+H2O → H2+CO2(H2/CO比の調整) (11) (シフト反応)
CO+2H2 → CH3OH +90 .97kJ/mol(発熱) (12) (メタノール合成反応)
ここで、(12)式のメタノール合成反応は、アンモニア合成の場合と同じく、低温高圧ほど進みやすい。従って、プラント構成、反応器ともアンモニア合成と類似したものになる。1913年,BASF社は、各種の触媒存在下、100気圧以上の高圧のもとで水性ガス(CO,H2より成る)を300~400℃で処理し、アルコール、アルデヒド、ケトンなどの液状混合物を得た。その後、反応条件を整え、主生成物をメタノールとすることに成功し、一九二三年、年産3000トンの工場をドイツ東部のロイナに建設した。200気圧、400℃、触媒はミタッシュが選んだZnO-Cr2O3系であった(メタノール合成には、現在はCu?O-ZnO系触媒を用いる低圧法が多く採用されている)。
ボッシュの伝記作者はこのメタノールについて記している。「BASF社の研究活動によって、再び一つの製品が天然の座から追い出されました。丁度五〇年前に
茜
の根からのアリザニンが合成アリザニンによって追い出されたように、25年前にインドの天然
藍
が合成藍(インジゴ)によって駆逐されたように、合成アンモニアが天然のチリ硝石より専売的立場を奪ったように、メタノールの合成的製造とともに今日まで木材乾留の副産物として少量得られていた木精は全く背後に押しやられました。合成メタノールは安いばかりでなく無限に作る事が出来ます」a)。ボッシュは、1923年の夏にはメタノールの自動車用燃料としての評価実験も実施している。現在メタノール車は一般には普及していないが、世界的に著名なモータースポーツの一つであるインディカーシリーズでは、メタノールが1928年から使われ、1965年にはその使用が義務化されて、2006年に再生可能であり
炭素
中立
とされる発酵法バイオマスエタノール主体に替わるまで長い間用いられた。アルコール類は、オクタン価が高いので圧縮比を高く、即ち熱効率を高くできるからである。いうまでもなくメタノールは現在も代表的な化成品原料のひとつである。また、水素利用の媒体水素利用の媒体(最近ではアンモニアもその一つに擬せられている)、燃料電池の燃料、C1化学の中核的化合物としても期待されるものであり、化石燃料ではなくバイオマスからのガス化、化学合成による製造も試みられている。
ちなみに、上述のとおりメタノールは合成ガス(COと水素を主成分とする混合ガス)からの化学合成でつくられるが、一方エタノールは現在、飲料また運輸用にはグルコースからの生物化学的発酵、工業用にはエチレンの水和に多くよっている。合成ガスを用いた化学反応でのエタノール合成が難しいのは、C-O結合をそのままに維持することに加えて、メタノール合成の場合とは異なり、C―C結合をつくるため、C-O結合の解離反応を同時に生起させねばならず、不可能ではないが、触媒(Rhなど)の高度な制御が必要となるからである。
1920年代には世界のエネルギー供給の九割は石炭が担っていた。ボッシュは、石炭からガソリンなどの燃料を製造することが、二十世紀最大の利益を生む新しい技術になると信じ、ベルギウス法を用いた人工ガソリン合成、即ち石炭を原料にした高圧での水素添加プラントの開発にも力を注いだ。ただ、アンモニア合成の場合のような気体ではなく、取り扱いの厄介な原油と石炭のスラリーが対象であり、幾多の技術的困難があった。ロイナ工場で褐炭の液化プラントが、BASF社を含む九社の合同企業IGファルベンの事業として稼働を開始したのは1927年である。開発開始当初は早晩石油が不足し、値上がりするとの予測であったが、1920年代の米国での油田発見、1929年の世界大恐慌で、一時事業は危うくなった。その後、様々な経緯をへて、第二次世界大戦中ではドイツに必要なガソリンの大部分を供給することができた。航空用ガソリンについては95%が石炭原料、水素添加の合成石油であった。
ボッシュは、アンモニア合成などの「高圧化学反応法の開発と改良への貢献」で、1931年にベルギウスとともにノーベル化学賞を受賞した。純正科学者ではない技術者の工業的業績での受賞は異例であった。ただ、ボッシュと同時期にBASFに勤務した特許部長が著した邦訳で350頁にも及ぶボッシュの評伝a)は、そのために特に項目を設けることもなく、受賞に関する記述は、折からの経済恐慌に対する経営者としての様々な苦労の間の一挿話として、授賞理由とボッシュの講演趣旨を含め二頁の簡潔なものである。
ハーバー、ボッシュその後
以上、人類の記念碑的事業ともいえるアンモニア合成の研究開発、工業化は、ドイツの科学技術隆盛の時期のことであり、登場人物にはノーベル賞受賞者も少なからず含まれる。平和な時代であれば、彼らは充実した穏やかな研究者人生、技術者人生を全うしたかも知れないが、第一世界大戦、その後のヒットラー・ナチス台頭のドイツで、多くは苦難の道を歩むこととなった。特に、ユダヤ人であり熱烈な愛国者でもあったハーバーの劇的人生については多くの評伝があり、科学、科学者と戦争また国家との関わりに考えを巡らせる、過酷ではあるが相応しい素材となっている。ボッシュも、第一次世界大戦でハーバー・ボッシュ法によるアンモニアからの硝酸爆薬が多量に使用されたことを念頭に、ヒットラーが政権に就く直前の1932年、こう発言している「これが成功しなかった方が良かったのではないかと何度か考えたことがある。そうすれば戦争はもっと早く終わり、損害も少なかったのではないか。紳士諸君、こうした疑問はすべて無意味だ。科学と技術の進歩は止められない」。ヒットラーに批判的であったボッシュはナチスドイツの崩壊を待たず、1940年に世を去った。
まとめ、温暖化問題に及ぶ
既に記したように、十九世紀末の1898年、クルックス卿は英国アカデミー協会の会長就任に当たり次の趣旨の演説を行った。「英国をはじめすべての文明国家は、来たるべき人口増と食糧難で、生死の危機に瀕している。ただ、この暗黒の中にも一条の光はある。それは空気中の窒素の固定である。窒素からつくられるアンモニアは肥料のもととなり、また硝酸は火薬の原料になる。これこそ化学者の才能に待つべき偉大な発明の一つである」。この要請を受けて8年後には、科学者・技術者らの多大の労苦によってハーバー・ボッシュによるアンモニア合成法が開発工業化され、当面の食料危機は乗り切ることができた。
この演説から120余年後の今日、照らし合せて想起されるのは、このままでは危機的とされる気候変動問題であり、それに対する科学技術者への期待である。一時期、人口増、エネルギー消費量増大にともなう化石燃料の枯渇、或いは限定的に良質・廉価な石油供給の逼迫も、また同様のニュアンスで捉えられていたこともあったが、最近はそれをはるかに優越して、気候変動、地球温暖化問題である。そして周知のとおり、化石燃料の燃焼によって生成するCO2がその原因に擬せられ、低炭素社会から、さらに進んで早期に脱炭素社会へといわれる。
もとより、クルックス演説と状況は似ているようで、大きく異なる。具体的には危機の認識、また対策技術の明確性などである。
クルックス卿の認識、即ち、産業革命後の欧州の人口増に、食料供給が追い付かない状況は、当時は危機感として多くの人々がもっていたものと思われる。もっとも、この演説が評判になってから、クルックス卿の挙げた数値を疑い、
徒
に危機を煽るものとして反対する意見もあった。例えば、当時の窒素肥料の元であるチリ硝石の利用可能量は無限に近いというものである。今もCO2による温暖化に疑義を呈する人がない訳ではないのと似ている。ただ、クルックス卿の言う恐れは一般人にも容易に理解可能であったろうが、温暖化の方は、一般人は勿論、直接の関与者以外は科学者、技術者でさえ自身で評価することは難しい。
また、対策技術については、クルックス卿は「暗黒のなかにある一条の光」を、空中窒素の固定と特定し、主たる責任担当を化学者と指定してさえいる。一方、CO2問題は、複雑多様なエネルギー問題そのものであり、課題、対策技術もそれぞれで、特定の一つの技術が解決とはなり難い。また、エネルギー分野の技術は、それほど意表をつくような妙案が考えられる訳ではない。熱力学や物理化学の厳たる制限もあり、加えてハーバー、ボッシュの時代が物理化学、熱力学の勃興、成長期であったに対し、今は科学技術の成熟した状況との事情もある。さらにはことの性格上、特定の国、地域だけではなく、世界全体としての課題であって、もとよりクルックス卿の念頭にあった英国・欧州の先進国のみのことではない。実験室での科学的、技術的革新があっても、これを要請されている時間の制限の中で、実用的なシステムとして成立させ、商用ベースに乗せて、速やかに遍く世界へと拡げねばならない。主要部分が簡単な化学式で書くことができ、エネルギー的にも適切なプロセスだからといって、それが実際に世に出るまでには筆舌に尽くしがたい努力と時に幸運さえ必要なことは、ハーバー・ボッシュのアンモニア合成プラント開発の例を引くまでもなく自明のことであろう。
これらの背景には、勿論120年間の大きな世界情勢の変化がある。十九世紀末、当時世界人口は約16億人、使用エネルギーは石油換算で約二億トンであったが、現在でそれぞれ5倍、70倍と急増している。高度な文明社会とはなったが、国際情勢も複雑化して、諸国間の対立も厳しい。技術は人々の生活をより良く豊かにするための有用な一手段であるが、以前は人々の求めるものが直接的であり、必要な技術も個別的でまたその効果、弊害も判りやすかったが、今ではその明確性は薄らいでいる。諸々の課題、その解決策も単純ではなくなることは当然とも言える。
今、時代は大きく移ろうとしている。脱炭素社会をめざして、石炭、石油、天然ガスなどの化石燃料の利用を早期に抑制し、さらには停止しようとする動きにある。ただ、それが具体的に今後どのように進展していくか、どのような技術、システムが中核となり、どのような時間的経緯で進んでいくか、予測には誰しも困難を感じるところであろう。例えば、もし現今いわれる風力・太陽光発電などの再生可能エネルギーからの水素、或いはその水素を用いた本項の主題たるアンモニアが、化石燃料に変わって発電用などに世界中で使用されることになれば、50万年前といわれる火の発見以来、木材、石炭、石油・天然ガスと変遷してきた炭素系燃料にかわる、人類はじめての非炭素系燃料の大掛かりな利用ということになる。アンモニア合成の工業化を成し遂げたボッシュが、化石燃料の中で最も埋蔵量豊富な石炭からの人工ガソリン合成の開発に執念を燃やしてから、わずかというべきか、既にというべきか100年である。彼が今日いればどのような感慨を持つか興味なしとしない。
ともあれ、エネルギー利用の低炭素化から脱炭素に進む大きな時代の流れは、今後も止まることはなく、そのための再生可能エネルギー利用拡大の必要性は、世界の共通の認識であろう。ただ、太陽エネルギーの無限性を強調して、将来はこれを電力に変換し、今石油などの化石燃料に頼っている有機物もすべてそれからの水素をもとにつくる、確かに数段のプロセスの過程で、効率は下がってしまうが、太陽エネルギーは無限にあるのだからその分はさらに供給すればいい、という意見も時にみられる。それが将来現実的に可能か否か、また望ましい手法か否は別にして、エネルギー利用の贅沢を差し控える、という発想なくしては将来は危ういであろう。即ち省エネルギー、節約は確実に低炭素になるが、逆に低炭素、特に脱炭素にまで及ぶと省エネルギー、節約になるとは限らない。その目的とするところ、対応手法が異なるから当然のことである。
「科学と技術の進歩は止められない」と、晩年のボッシュは様々な感懐を込めて言明した。科学、技術の本質的性格ではあり、また別よりすれば科学技術は常に中途にして半端とも看られるが、それにしてもその速度と内容にはおのずから制限がある。科学技術は万能ではなく、人間の限りない欲望をみたすことは不可能であり、抑々科学技術はそのような使命をもつものではないことは、特に今日のような時代の転換期においては強く心に留めておくべきものと思われる。
クルックス卿は食料危機の解決の担い手として化学者を特に指名、鼓舞したが、現在、世上に挙がる脱炭素のための技術テーマをみても、化学の果たす役割が大きいことは明らかであろう。化学技術者は十八世紀末の本格的近代化学発生の時から、特にここに述べたボッシュの時代から、石炭、石油の利用技術をはじめとするエネルギー、またそれに連動した環境技術の進展に深く
与
り、さまざまな成果をあげてきた。分野により濃淡はあろうが、「歴史を知れば未来が見える」とは、エネルギー問題についてなじみやすい標語と思われる。個別的な技術の重要度、開発普及の難易の判断は勿論であるが、全体を俯瞰し、歴史を踏まえて将来を予見するために、化学技術者の素養、基礎知識、経験がおおいに役立つはずである。温暖化をはじめとするエネルギー・環境問題は、今後どのように進展しようと短期間で解決してそれで終わるような課題ではなく、また程度の差こそあれ化学の関与しない具体的課題もない。特に若い諸君には、平凡ながら、まずは自ら考え、良質の研究課題を策定し選んで、日々精進することを期待したい。
主な参考資料
・カール・ホルダーマン「カール・ボッシュ、その生涯と業績」、和田野基訳、文陽社(1964年)、
・ジョン・パーリン「森と文明」、安田喜憲、鶴見清二訳、晶文社(1994年)
・トーマス・ヘイガー「大気を変える錬金術、ハーバー、ボッシュと化学の世紀」、渡会圭子訳、みすず書房(2010年)
・清山哲郎、浅見章晴、江崎正直「二十一世紀は化学の時代、翔け!化学技術者」、清山哲郎先生遺稿本刊行会(1998年)
・宮田新平、「愛国心を裏切られた天才」朝日新聞社・朝日文庫(2019年)
・大西孝治「触媒―その秘密を探る」、大日本図書(1977年)
・マノロフ「化学を作った人々(下)」、早川光男訳、東京図書(1,979年)
・井本稔ほか編「化学のすすめ」、筑摩書房(1,971年)
・長哲郎編「NOxの化学」、共立出版(株)(1,978年)
文中引用
a)上掲「カール・ボッシュ、その生涯と業績」
b)日本国公表特許公報、特表2,002-512,934
c)「幕末維新パリ見聞記」井田進校注、岩波文庫(2,009年)
引用図
図1、3 上掲「二十一世紀は化学の時代、翔け!化学技術者」
図2 長倉三郎・竹内敬人ほか「化学?」、東京書籍(2,003年)
|